用于组织重建的I型胶原支架通常具有受损的机械特性,例如刚度有限和缺乏强度。本研究提出了一种新技术,通过用浓缩盐溶液处理来微调胶原蛋白支架的刚度和生物降解性。胶原蛋白支架通过铸造、冷冻和冻干过程制备。支架用90%饱和盐溶液处理,盐取自Hofmeister系列,然后进行化学交联。用由二价阳离子和一价阴离子组成的盐处理,例如CaCl2,导致支架快速收缩至原始表面积的约 10%。有效盐主要在霍夫迈斯特系列的离液末端。收缩的支架比不收缩的对照支架硬10倍以上,并且显示出孔径减小和肿胀,组织较少的胶原纤维。这种效应可以精确到单个胶原蛋白分子的水平,并表明收缩效应是由三螺旋内稳定氢键的破坏驱动的。钙中无钙沉积物2处理过的支架。与H相比,大鼠皮下植入显示出相似的生物相容性2O和NaCl处理支架,但减少了细胞内流并增加了结构完整性,3个月后没有显着降解的迹象。综上所述,高浓度离液盐可用于调节胶原支架的力学特性,而不影响生物相容性。该技术可用于再生医学中,以加强胶原蛋白支架以更好地顺应周围组织,但也可用于例如缓释药物输送系统。
氯化钙的刚度2、氯化钠和氢2用PIUMA纳米压头测量O处理过的胶原蛋白支架(Optics11,荷兰阿姆斯特丹;图 3A)。16在测量之前,将支架在PBS中孵育30分钟,然后在PBS中的60%牛血清白蛋白中进行5分钟的钝化步骤,以防止探针粘附在支架上。每个样品在25×1 mm的网格中进行1个压痕,单个压痕之间的距离为200μm(图3B)。对于软样品,压头探头的刚度为 0.05 N m−1对于较硬的样品,使用刚度为 0.47 N m 的探头−1.两个探头的直径均为180μm。压痕深度,以 5 μm s 的速度达到−1,为15μm,探针保持在原位2秒(压痕时间)。每种脚手架类型独立测量3次。
使用纳米压痕评估刚度(图3)。氯化钙2、氯化钠和氢2O处理过的支架独立测量三次,每个支架在不同位置有25个压痕(图3B)。氯化钙2脚手架 (7.4 × 103Pa)比NaCl更硬(1.2×103帕)和H2O 处理支架 (4.4 × 102Pa)如(图3C)所示。峰值显示刚度大于 3.0 × 104Pa,最有可能的是当正好凹进在多孔支架中的胶原蛋白结构顶部时,表明CaCl的刚度2处理过的胶原蛋白材料高于 7.4 × 103帕。



Piuma是功能强大的台式仪器,可探索水凝胶、生理组织和生物工程材料的微观机械特性。表征尺度从宏观直至细胞。专为分析测试软材料而设计,测量复杂和不规则材料在生理条件下的力学性能。杭州轩辕科技有限公司
●内置摄像镜头,方便实时观察样品台
●实时分析计算测量结果,原始数据并将以文本文件存储,方便任何时候导入Dataviewer软件进行复杂处理
●探针经过预先校准,即插即用。对于时间敏感的样品确保了快速测量
●光纤干涉MEMS技术能够以无损的方式测量即使是最软的材料,并保证分辨率。同时探针可以重复使用Piuma轩辕纳米压痕仪Piuma轩辕纳米压痕仪
| 模量测试范围 | 5 Pa - 1 GPa |
| 探头悬臂刚度 | 0.025 - 200 N/m |
| 探头尺寸(半径) | 3 - 250 μm |
| 最大压痕深度 | 100 μm |
| 传感器最大容量 | 200 |
| 测试环境 | air, liquid (buffer/medium) |
| 粗调行程 | X*Y:12×12 mmZ:12 mm |
加载模式 |
Displacement / Load* / Indentation* |
| 测试类型 | 准静态(单点,矩阵) 蠕变,应力松弛 DMA动态扫描(E', E'', tanδ) |
| 动态扫描频率* |
0.1 - 10 Hz |
| 内置拟合模型 | Young's Modulus (Hertz / Oliver-Pharr / JKR) |
| *为可选升级配置 |
|
新型光纤干涉式悬臂梁探头,利用干涉仪来监测悬臂梁形变。
创新型光纤探头,弥补了传统纳米压痕仪无法测试软物质的问题,也解决了AFM在力学测试中的波动大,操作困难、制样严苛等常见缺陷。
●背景噪音低:激光干涉仪抗干扰强于AFM反射光路
●制样更简单:对样品的粗糙度宽容度高于AFM
●刚度选择更准确:平行悬臂梁结构有利于准确判别压痕深度与压电陶瓷位移比例关系,便于选择合适刚度探头来保证弹性形变关系的稳定性,进而获得重复率更高、准确性更好的数据
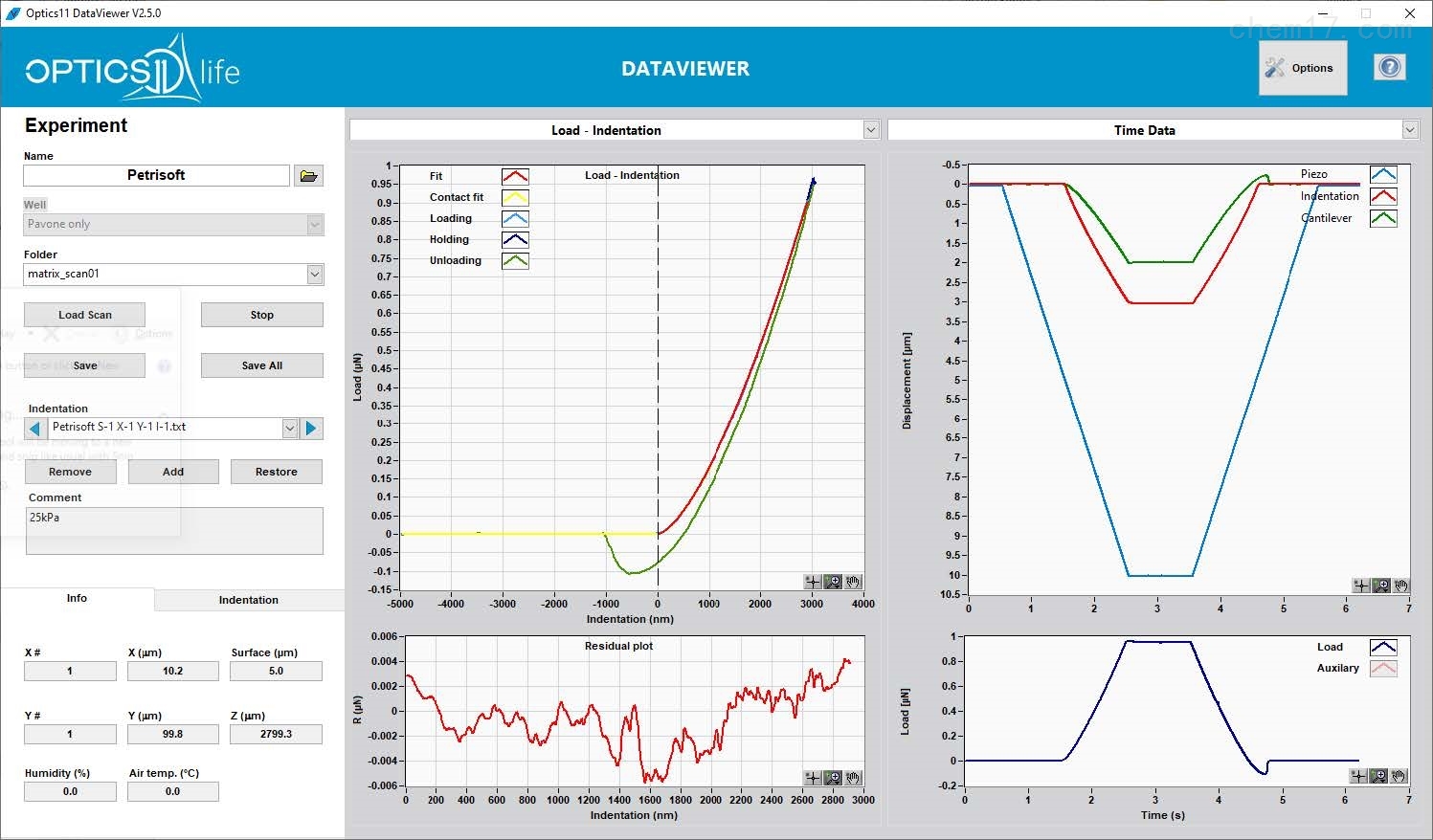
●借助功能强大而易于操作的软件,用户可以自由控制压痕程序(载荷、位移等)。自动处理曲线的流程,可以获得数据和结果的快速分析
●原始参数完整txt导出,便于后续复杂处理的需要
●利用Hertz接触模型从加载部分计算弹性模量,与常用的Oliver&Pharr方法相比,更为适合生物组织和软物质材料特性
| 年 份 | 期 刊 | 题 目 |
|---|---|---|
| 2022 | Advanced Functional Materials | Engineering Vascular Self-Assembly by Controlled 3D-Printed Cell Placement |
| 2022 | Biomaterials | Hydrogels derived from decellularized liver tissue support the growth and differentiation of cholangiocyte organoids |
| 2021 | Biofabrication | 3D bioprinting of tissue units with mesenchymal stem cells, retaining their proliferative and differentiating potential, in polyphosphate-containing bio-ink |
| 2021 | nature communications | Janus 3D printed dynamic scaffolds for nanovibration-driven bone regeneration |
| 2020 | Environmental Science & Technology | Effect of Nonphosphorus Corrosion Inhibitors on Biofilm Pore Structure and Mechanical Properties |
| 2020 | Acta Biomaterialia | A multilayer micromechanical elastic modulus measuring method in ex vivo human aneurysmal abdominal aortas |